I filtri respiratori oppongono una effettiva barriera per impedire le contaminazioni crociate tra pazienti, circuiti per ventilazione, ventilatori o stazioni per anestesia, e l'ambiente ospedaliero. Il loro utilizzo è ampiamente riconosciuto e il loro impiego è raccomandato da numerose Società di Anestesia(1). Sono utilizzati in molti reparti ospedalieri, in particolare nelle sale operatorie, nelle unità di terapia intensiva, nei reparti di Pneumologia e negli ambulatori di funzionalità respiratoria.
Gli scambiatori di calore e umidità (HME) minimizzano la perdita di umidità attraverso l'espirato del paziente e combinati all'azione filtrante (HMEF) riducono i rischi di contaminazione crociata nell'ambiente ospedaliero.
Pagine correlate
- Filtrazione e Umidificazione
- Filtri respiratori
- HME e HMEF
- Filtri per dispositivi respiratori
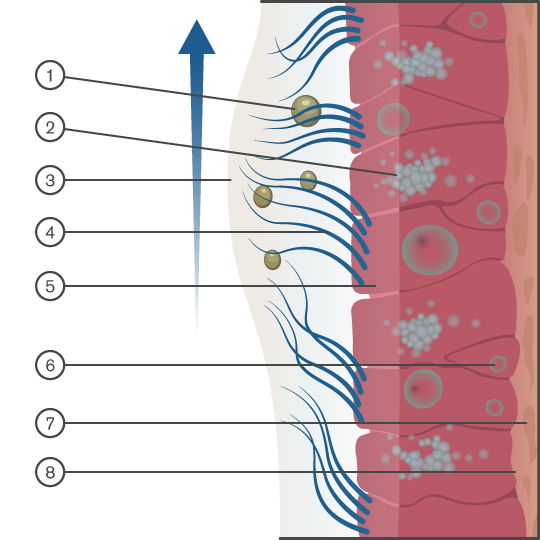
Movimento del muco verso la faringe
La funzione naturale delle vie aeree superiori è filtrare, umidificare e riscaldare l’aria inspirata. L’aria viene riscaldata passando sopra un’ampia rete di capillari nel naso. Le membrane mucose che rivestono le vie aeree superiori contribuiscono a umidificare l’aria ed a intrappolare particelle trasportate dall’aria (polvere e microbi). Le cilia spostano il muco dai polmoni verso la faringe, dove viene eliminato.
Le vie aeree superiori contribuiscono anche a conservare calore e umidità, che altrimenti andrebbero perduti durante la respirazione. I gas che lasciano i polmoni durante l’espirazione hanno una temperatura corporea (37°C), un’umidità assoluta (AH) di 44 mg/l e un’umidità relativa (RH) del 100%. Quando il paziente espira, le vie aeree superiori trattengono calore e umidità, trasferendoli poi ai gas inspirati, che generalmente sono più freddi e più secchi a seconda delle condizioni ambientali. L’ampia superficie delle vie aeree superiori le rende particolarmente efficienti, contribuendo a ridurre gli effetti negativi dell’inalazione prolungata di gas freddi e secchi.
Questa protezione fisiologica naturale viene bypassata quando si inserisce un dispositivo per le vie aeree artificiale quale ad esempio: tubo tracheale, dispositivo sovraglottideo o una cannula tracheostomica. Di conseguenza la fonte di gas freddi e secchi raggiunge direttamente i polmoni, che sono sensibili e delicati, aumentando il rischio di infezioni e potenziali contaminazione microbica.
L’inalazione prolungata di gas medici freddi e secchi può inoltre provocare il raffreddamento delle vie aeree e la disidratazione delle superfici musose. L'aria ambiente in una stanza è normalemente di 23°C con umidità relativa (RH) del 60% e umidità assoluta (AH) di 21mg/l. I gas medicali sono solitamente a 10-15°C con RH del 0-2 % e AH di 0.5 mg/l, ciò potrebbe comportare l'ulteriore rischio di danneggiamento delle cilia, ispessimento del muco, rischio di infezione, formazioni di croste con conseguente aumento di rischio di occlusione del tubo, atelettasia ed infine, costi più elevati dovuti ad una degenza ospedaliera prolungata.
Legenda: 1. Particolato. 2. Cellula mucosa 3. Strado di muco 4. Cilia 5. Cellule epiteliali colonnari. 6. Cellula staminale 7. Lamina propria 8. Membrana basale
Ambiente ospedaliero
Infezione
Protezione del paziente
I pazienti in condizioni critiche con un’immunità ridotta sono generalmente esposti a un rischio maggiore di infezioni. Queste infezioni nosocomiali comportano un aumento della morbilità e della potenziale mortalità, oltre ad avere un impatto significativo sui costi di trattamento del paziente a causa di un prolungamento della degenza ospedaliera. L’uso strategico di un filtro respiratorio efficiente e correttamente validato fornisce una barriera efficace tra il paziente, i circuiti respiratori e le apparecchiature respiratorie, riducendo il rischio di contaminazione crociata.
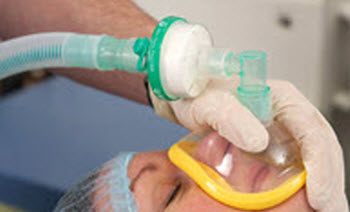
Contaminazione crociata
Protezione del sistema respiratorio
I pazienti che necessitano di una via aerea artificiale vedono la loro protezione fisiologica naturale bypassata. Questo aumenta il rischio di infezione e di contaminazione crociata tra pazienti e apparecchiature sanitarie. La contaminazione crociata tra pazienti attraverso un sistema anestetico è stata già segnalata e documentata². Le principali aree di rischio includono Epatite C, Mycobacterium Tuberculosis, sangue nell’espettorato, SARS e Coronavirus o simili.
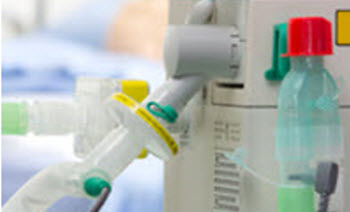
Protezione delle apparecchiature respiratorio e dell'ambiente ospedaliero
Protezione delle apparecchiature
L’uso di filtri respiratori adeguati ed efficaci può proteggere apparecchiature delicate e costose, contribuendo a preservarne la funzionalità, ridurre i costi di gestione e diminuire il rischio di contaminazione crociata.
Efficienza comprovata
Sempre più spesso, l’unico modo per consentire al'operatore sanitario di determinare l’efficienza e l’efficacia di un filtro respiratorio, HME o HMEF è attraverso protocolli di test standardizzati e i relativi risultati. È fondamentale che i dati siano clinicamente pertinenti, aggiornati e rappresentativi del prodotto effettivamente utilizzato dal cliente.
La nostra gamma di filtri respiratori e HMEF è stata testata in modo indipendente e ha dimostrato un’elevata efficienza nel prevenire il passaggio di batteri e virus. Questi test forniscono informazioni clinicamente rilevanti per decisioni basate sull’evidenza riguardo al prodotto più appropriato per soddisfare le esigenze cliniche.
Test microbiologici
Tutti i nostri filtri vengono testati in laboratori specializzati di microbiologia contro prove batteriche e virali clinicamente rilevanti. Tali test vengono generalmente eseguiti da strutture indipendenti che sviluppano protocolli specifici per simulare le condizioni a cui un filtro può essere esposto in un ambiente ospedaliero.
Viene scelta una particella di prova che simula la dimensione dei batteri e virus più comuni. Ogni filtro e HMEF Intersurgical viene testato singolarmente e ne viene verificata la performance.
I test clinicamente rilevanti sono effettuati su tutti i prodotti utilizzando Bacillus subtilis (1,0 µm × 0,7 µm) e il batteriofago Ø174 (0,027 µm).
Virus potenzialmente infettivi [Dimensioni delle particelle insizes μ microns (μm)]

1. Colifago T1 [0.017μ]
2. MS-2 colifago [0.02μ]
3. Epatite C [0.03μ]
4. Adenovirus [0.07μ]
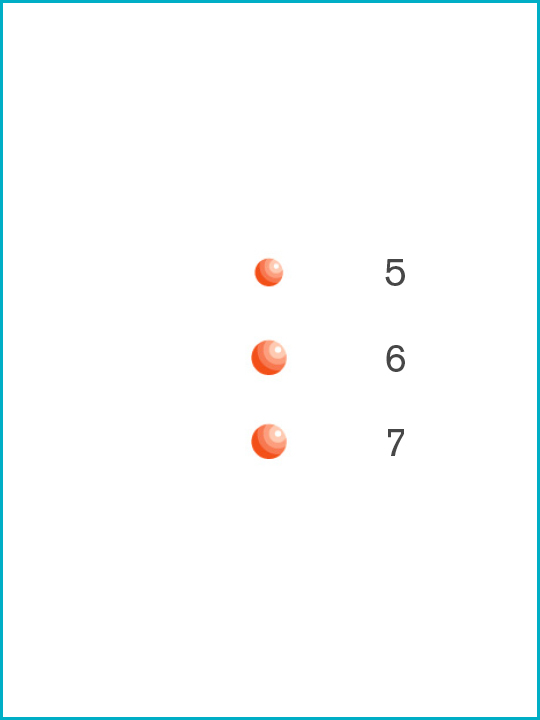
5. HIV [0.11μ]
6. Orthomyxovirus [0.1μ]
7. Citomegalovirus (CMV) [0.1μ]
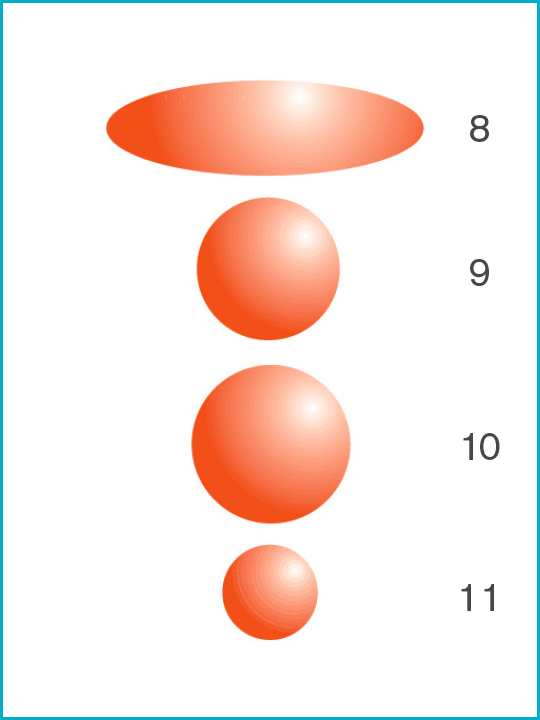
8. Mycobacterium tuberculosis [0.3μ x 1.0μ smallest size]
9. Serratia marcescens [0.45μ]
10. Pseudomonas aeruginosa [0.5μ]
11. Brevundimonas diminuta [0.3μ]
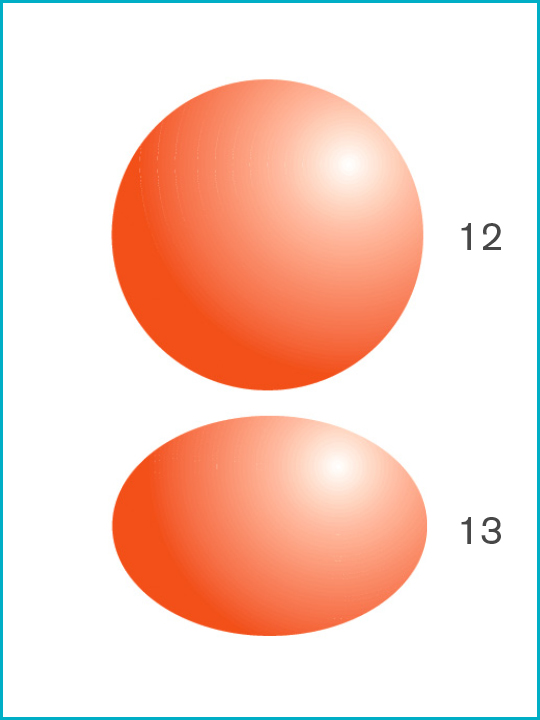
12. Staphylococcus aureus [1.0μ]
13. Bacillus subtilis [1.0μ x 0.7μ]
Il livello di passaggio delle particelle durante il test determina l’efficienza del filtro. Tale efficienza viene espressa come percentuale basata sul rapporto tra particelle testate e la carica di prova.
| Numero di organismi sottoposti al filtro | Numero di organismi che attraversano il filtro | Efficienza del filtro |
| 100,000 | 1000 | 99% |
| 100 | 99.9% | |
| 10 | 99.99% | |
| 1 | 99.999% |
L'inoculo di sfida previsto nel protocollo di test virale (batteriofago φ174, 0,027 µm) è severo almeno quanto quello posto dal Coronavirus (COVID‑19). Le dichiarazioni di performance sono disponibili su richiesta per i singoli prodotti.
L’epidemia COVID‑19 ha colpito duramente molti Paesi e causato migliaia di decessi a livello globale.
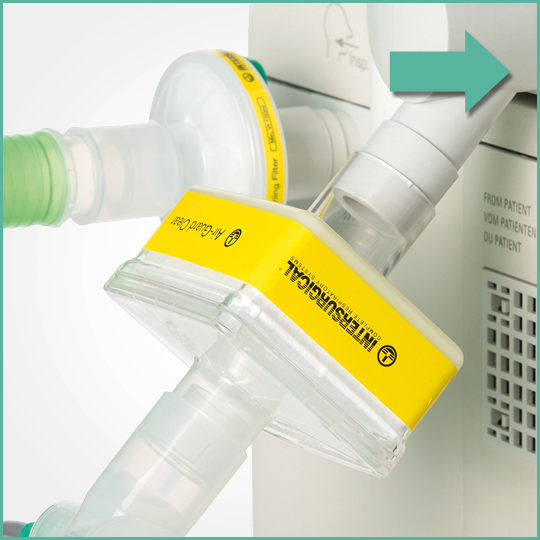
La gamma di filtri respiratori e HMEF Intersurgical è stata testata in modo indipendente e ha dimostrato un’elevata efficienza nel prevenire il passaggio di batteri e virus in ambiente sanitario.

Tutti i prodotti dotati di filtro sono stati testati e sono conformi ai requisiti della norma ISO 23328-2003.

Sulla base delle dimensioni del virus SARS-CoV‑2 (0,05–0,1 µm) e dei dati di test più severi disponibili, utilizzando una particella di 0,027 µm, è possibile confermare che la gamma Intersurgical offre almeno lo stesso livello di protezione anche contro il COVID‑19 come riportato nei test microbiologici indipendenti. Copie disponibili su richiesta.
Codifica a colori per facilitare la selezione
La nostra gamma di filtri respiratori, scambiatori di calore e umidità (HME) e filtri scambiatori di calore e umidità (HMEF) è codificata per colore per facilitare l'identificazione e garantire l'uso corretto del filtro/HME, riducendo al minimo i potenzilai rischi per il paziente.
Riferimenti 1: Association of Anaesthetists of Great Britain and Ireland 1996. Danish Society of Anaesthetists 1998. French Society of Anaesthetists 1998
Riferimenti 2: Chant K, Kociuba K, Munro R, et al. Investigation of possible patient-to-patient transmission of hepatitis C in a hospital. NSW Public Health Bull 1994; 5:47-51.